Dunnedarmtransplantatie
Algemeen
Dunnedarmtransplantatie (DDTx) is sinds de 60er jaren sporadisch uitgevoerd bij mensen. Sinds de komst van tacrolimus en andere immunosuppressiva begin jaren negentig zijn de resultaten sterk verbeterd en is DDTx geen experimentele behandeling meer, maar een standaardbehandeling voor patiënten met darmfalen bij wie totale parenterale voeding (TPV) faalt.
DDTx heeft daarmee dezelfde status als andere solide orgaantransplantaties (hart, longen, nier, lever en pancreas). Het aantal darmtransplantaties zal altijd laag zijn in vergelijking met lever- of niertransplantatie. De oorzaak hiervoor is de relatieve zeldzaamheid van chronisch darmfalen en thuisTPV (in Nederland ongeveer 300 patiënten).
Tot 2010 zijn er wereldwijd ruim 2000 darmtransplantaties verricht, het merendeel in de Verenigde Staten. In Nederland zijn tot op heden (2010) 11 darmtransplantaties verricht. Het UMC Groningen is het enige centrum in Nederland waar DDTx uitgevoerd wordt. Ongeveer de helft van de DDTx vindt bij kinderen plaats.
Indicaties
De belangrijkste indicatie voor DDTx is falende TPV bij permanent darmfalen. Darmfalen wordt gedefinieerd als het onvermogen tot enterale voeding waarbij >75% van calorische behoefte via TPV wordt toegediend voor een periode van meer dan 3 maanden. Bij permanent darmfalen is er sprake van irreversibiliteit en is enterale voeding (grotendeels) niet mogelijk. De oorzaken hiervoor kunnen anatomisch of functioneel zijn (zie tabel 1)
Tabel 1: Oorzaken van permanent darmfalen bij ontvangers van een darmtransplantatie
| Kinderen | Volwassenen | ||
|---|---|---|---|
| Gastroschisis | 21 % | Ischemie | 24 % |
| Volvulus | 17 % | Ziekte van Crohn | 14 % |
| Necrotiserende enterocolitis | 12 % | Trauma | 10 % |
| Retransplantatie | 8 % | Desmoid tumor | 9 % |
| Intestinal atresie | 8 % | Motiliteitsstoornis | 8 % |
| Pseudo-obstruction | 9 % | Volvulus | 7 % |
| Aganglionosis/Hirschsprung | 7 % | Dunnedarm overig | 9 % |
| Microvillus inclusion disease | 6 % | Retransplantatie | 6 % |
| Malabsorptie overig | 3 % | Gardner syndroom | 3 % |
| Dunnedarm overig | 5 % | Tumor overig | 5 % |
| Motiliteitsstoornis overig | 1 % | Overig | 5 % |
| Tumor | 1 % | ||
| Overig | 2 % | ||
Falen van TPV kan onderverdeeld worden in verschillende oorzaken:
- Leverschade (fibrose/cirrhose) als gevolg van TPV. Vroeger werd dot TPN-induced liver disease genoemd, tegenwoordig wordt gesproken van Intestinal Failure Associated Liver Disease (IFALD) aangezien niet alleen TPV-componenten verantwoordelijk zijn voor leverschade
- Verlies van centrale veneuze toegang of shuntmogelijkheden voor toediening van TPV.
- Recidiverende. Levensbedreigende lijnsepsis
- Sterk gereduceerde kwaliteit van leven
Technische aspecten
In Nederland worden alleen postmortale donoren gebruikt. Gezien het lage aantal potentiële ontvangers is het niet nodig een levende donor bloot te stellen aan de risico’s van een partiële dunnedarmresectie. Bovendien zijn de uitkomsten van DDTx van levende of postmortale donoren gelijk.
Ongeveer 60% van de darmtransplantaties zijn geïsoleerde dunnedarmtransplanties. Vaak is echter een meervoudige transplantatie nodig. Bij IFALD of andere leverziekten kan een gecombineerde Lever-Darmtransplantatie plaatsvinden. Dit kan als een cluster met het pancreas (of een deel daarvan) als brug tussen dunnedarm en lever. Soms is een (pre-emptieve) niertransplantatie nodig bij chronische nierinsufficiëntie. Bij een kreatinineklaring beneden de 40 ml/min moet een niertransplantatie worden overwogen vanwege de noodzaak voor hoge spiegels tacrolimus na DDTx en een sterk verhoogd risico op nefrotoxiciteit op basis van tacrolimus.
Ook de maag kan in uitzonderlijke gevallen meegetransplanteerd worden. Lever-Maag-Darmtransplantatie wordt een multivisceral transplant (MVT) genoemd, Maag-Darm zonder Lever wordt een modified MVT genoemd. Het rechter hemicolon wordt meestal niet meegetransplanteerd bij volwassenen, bij kinderen wordt dit in toenemende mate wel gedaan vooral bij absorptiestoornissen als Microvillous Inclusion Disease. In dergelijke situaties is er minder diarree na transplantatie.
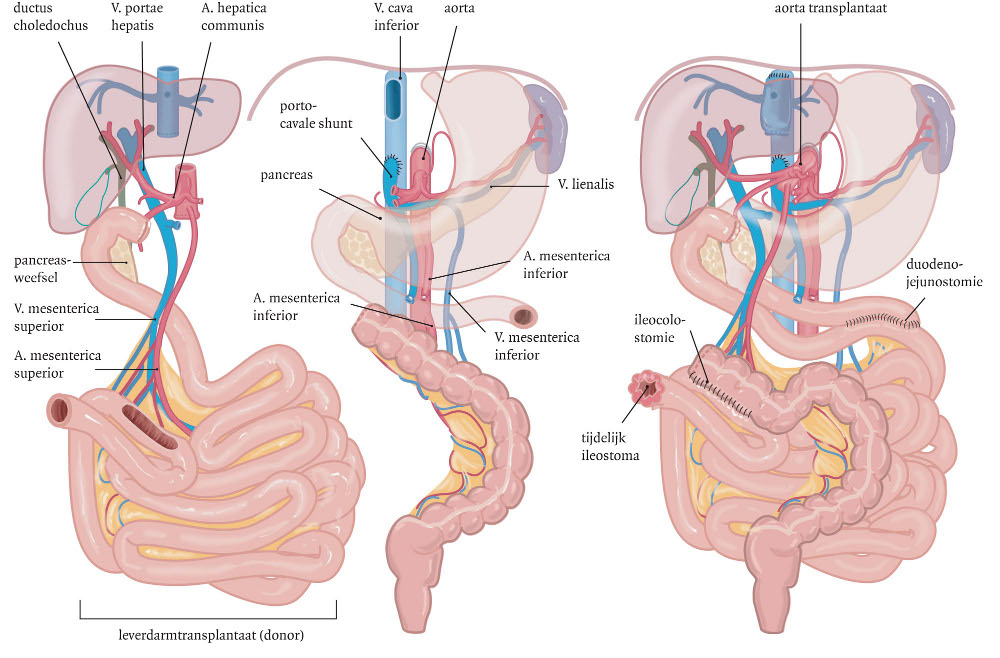
Een geïsoleerde dunnedarmtransplantatie wordt meestal met een systemische drainage op de vena cava aangesloten. De arteria mesenterica superior wordt op de infrarenale aorta aangesloten. De proximale darmanastomose tussen eerste jejunumlis van de ontvanger en de eerste jejunumlis van de donor. Het is belangrijk dat de eerste jejujunlis van de ontvanger lang genoeg is zodat bij rejectie en transplantectomie een jejunostoma kan worden aangelegd.
De distale anastomose wordt tussen het terminale ileum van de donor en het resterende colon (indien aanwezig) gelgede met een zgn. Bishop-Koop ileostoma (zie figuur NTVG 2005). Bij een Lever-Darmtransplantatie wordt een Piggyback-techniek gebruikt voor veneuze drainage. De arteriële anastomose wordt meestal via een supratruncaal aortaconduit gelegd. De darmanastomosen zijn gelijk aan die van een geïsoleerde DDTx (zie figuur NTVG 2005).
Figuur 1 Dijkstra et al NTVG 2005
Belangrijk!
Om bovengenoemde reconstructies mogelijk te maken is een voldoende lengte van de eerste jejunumlis voor een jejunostoma van groot belang. Bij een spoedenterectomie (bijv. bij arteria mesenterica trombose) moet de eerste jejunumlis in situ gelaten worden. Verder is het belangrijk om een vena cava inferior trombose te voorkomen om veneuze aansluitmogelijkheden te behouden. Lijnen in de vena iliaca hebben om deze reden niet de voorkeur. Ook plaatsing van stents of andere devices in de vena cava inferior of de vena iliaca moeten worden ontraden.
Resultaten darmtransplantatie
De 1 en 5 jaar transplantaat en patiënt overleving staan vermeld in figuur 2.
Figuur 2

De graft survival is afhankelijk van het type transplantatie zoals weergeven in figuur 3 voor volwassenen en in figuur 4 voor kinderen.
Legenda
| SBT | small bowel transplant | |
|---|---|---|
| MVT | multivisceral transplant |
| MMVT | modified multivisceral transplant | |
|---|---|---|
| SB+Liv | small bowel + liver transplant |
Figuur 3

Figuur 4

Bron: link 2023 ITR Report (https://intestinalregistry.org)
De resultaten van DDTx blijven iets achter in vergelijk met ander solide orgaantransplantatie. De belangrijkste oorzaak hiervan is afstoting. Hierdoor is relatief zware immuunspuppressie nodig met als gevolg infectieuze complicaties. De resultaten van DDTx in het UMCG zijn gelijk aan de resultaten in de literatuur.
Bij een geslaagde DDTx wordt de kwaliteit van leven als zeer goed ervaren. Kinderen die nooit hebben leren eten hebben veel tijd nodig om dit te leren. Volwassenen kunnen meestal binnen een maand na transplantatie normaal eten. Na transplantatie zijn er nog diverse re-interventies nodig zoals stoma opheffen, verwijdering van de centrale lijn en buikwandingrepen. De revalidatie na DDTx is ongeveer 6 maanden tot een jaar. In het eerste jaar na transplantatie worden patiënten vaak heropgenomen vanwege diarree, nierfunctiestoornissen en stomagerelateerde pathologie.
Immunosuppressie
Immuuninductie wordt gerealiseerd door methylprednisolon (Solu-Medrol) en Antithymocyten Globuline (ATG Fresenius) bij volwassenen en basiliximab (Simulect) bij kinderen voor reperfusie. Postoperatief wordt tacrolimus (Prograft) toegevoegd. Basiliximab wordt op dag 4 na transplantatie herhaald en de steroïden worden volgens vast schema afgebouwd. Afhankelijk van het bloedbeeld en nierfunctie wordt mycofenolaatmofetil (CellCept) gebruikt.Lange-termijn immunosuppressie bestaat uit prednison en tacrolimus, evt met mycofenolaatmofetil. Na transplantatie is het van groot belang of medicatiewijzigingen of -toevoegingen effect hebben op de immuunsuppressie. Vooral de tacrolimusspiegel kan veranderen door medicatiewijzigingen en -interacties. Ook dieetveranringen zoals grapefruit(sap) kunnen effecten hebben op de tacrolimusspiegel. Bij een te lage tacrolimusspiegel neemt de kans op rejectie snel toe. De darm is hierin anders dan lever of nier. Het is daarom gewenst om bij medicijnwijzingen of problemen altijd met het (kinder)transplantatieteam te overleggen.
Rejectie
Rejectie komt vaak voor na DDTx (35%) Rejectie kan ook laat (> 2 jaar) na transplantatie optreden. Hierin verschilt de darm van andere organen waarbij er eerder tolerantie ontstaat. De diagnose rejectie is vaak lastig te stellen op klinische gronden.
Veel voorkomende symptomen zijn algehele malaise, diarree, bloederige stomaproductie, koorts, ileus, leucocytose en septische verschijnselen. De meeste van deze symptomen zijn pas in een laat stadium aanwezig wanneer de rejectie moeilijk te behandelen is.
Subtiele veranderingen in stoma output en milde griepverschijnselen meten bij een DDTx ontvanger al reden zijn om aan rejectie te denken. De diagnose wordt gesteld op dunnedarmbiopten. Om deze reden worst meestal een Bishop Koop stoma aangelegd zodat eenvoudig biopten uit de getransplanteerde darm genomen kunnen worden.
Het stoma blijft meestal een jaar in situ omdat rejectie het meeste voorkomt binnen het eerste jaar. Na opheffen van het stoma is een coloscopie of gastroscopie nodig om biopten van het transplantaat te nemen. Feces calprotectine kan ook worden bepaald om te screenen voor rejectie, de gouden standaard is echter vooralsnog een dunnedarmbiopsie.
De behandeling van rejectie is moeilijk. De eerste stap is ophoging van de tacrolimusspiegel en bolussen steroïden. Als dit onvoldoende effect heeft wordt ATG gegeven. Als de rejectie therapieresistent blijkt is spoed-transplantectomie noodzakelijk om te voorkomen dat de patiënt overlijdt aan sepsis.
Follow-up
Patiënten blijven levenslang in follow-up in het UMCG. Meestal wordt gekozen om de follow-up samen met de verwijzende specialist uit te voeren. In de eerste maanden wordt wekelijks het bloed gecontroleerd inclusief de tacrolimusspiegels, de dosis wordt zo nodig bijgesteld.
In het eerste jaar er tenminste eens per 3-6 maanden een controle met scopie .Bij een stabiele situatie wordt er tenminste 1 x per jaar een scopie in het UMCG verricht. Vaak kunnen controles schriftelijk gedaan wordt waarbij het bloedonderzoek in een ziekenhuis dicht in de buurt wordt gedaan.
Na transplantatie is er een aanzienlijk risico op maligniteiten. Huidtumoren zijn zeer frequent, ontvangers moeten daarom zorgen voor adequate huidbescherming tegen zonnebrand. Ook posttransplantatie lymfoom (PTLD) komt voor (8-15%).
Darmtransplantatieteam UMCG
Bij vragen of twijfel verzoeken wij professionals laagdrempelig te overleggen met het darmtransplantatieteam. Er is altijd een (kinder)MDL-arts of transplantatiechirurg bereikbaar via de centrale van het UMCG.
Ook kunt u tijdens kantooruren altijd de darmtransplantatieverpleegkundige en diëtiste raadplegen door te mailen naar technischvoedingsteam@umcg.nl